|
АККУМУЛЯТОРЫ электрические (от лат. accumulator- собиратель,
накопитель), хим. источники тока многократного действия. При заряде от
внеш. источника электрич. тока в аккумуляторе накапливается энергия, к-рая при разряде
вследствие хим. р-ции непосредственно превращ. снова в электрическую и
выделяется во внеш. цепь. По принципу работы и осн. элементам конструкции
аккумуляторы не отличаются от гальванических элементов, но электродные р-ции,
а также суммарная токообразующая р-ция в аккумуляторах обратимы. Поэтому после разряда
аккумулятора может быть снова заряжен пропусканием тока в обратном направлении: на
положит. электроде при этом образуется окислитель, на отрицательном-восстановитель.
Наиб. распространены свинцовые аккумуляторы, часто наз. также кислотными. Их действие
основано на р-ции:
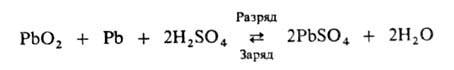
Электролит - р-р H2SO4 с концентрацией 12-24%
по массе в разряженном состоянии и 28-40% в заряженном. Напряжение разомкнутой
цепи (НРЦ) 1,95-2,15 В. Чаще всего применяют электроды из пасты, содержащей
смесь Рb3О4 и РbО с H2SO4 (активная
масса); эту пасту намазывают на профилированную сетку-токоотвод из сплава
Рb с 2-12% Sb. Электроды формируют, пропуская через р-р электролита зарядный
ток в определенном режиме; при этом на одном электроде образуется РbО2,
на другом-Рb. Затем электроды отмывают и сушат в условиях, исключающих
возможность окисления Рb. Аккумуляторы, собранные из таких электродов, после заливки
у потребителя р-ром H2SO4 готовы к эксплуатации без
подзаряда (остальные виды аккумуляторов требуют дополнит. заряда). Применяют также
панцирные электроды, в к-рых активная масса заключена в перфорированную
пластмассовую или тканевую трубку.
Первый свинцовый аккумулятор был создан Г. Планте в 1859. Сейчас более половины
мирового произ-ва Рb расходуется на изготовление свинцовых аккумуляторов с единичной
емкостью 2-5000 А * ч и уд. энергией 25-40 Вт * ч/кг. Осн. достоинства
таких аккумуляторов: относит. дешевизна, пологие разрядная и зарядная кривые, возможность
работать в разл. режимах разряда; недостаток - невысокий ресурс работы
(число допустимых циклов заряд-разряд для стартерных аккумуляторов 100-300, для тяговых
с панцирными электродами 800-1500). В конце заряда на электродах свинцового
аккумулятора наблюдается заметное выделение газов, к-рые часто увлекают за собой
туман из капель H2SO4. В связи с этим большое внимание
уделяется созданию герметизированных свинцовых акуумуляторов.
Щелочные никель-кадмиевые (НКА) и никельжелезные (НЖА) аккумуляторы по распространению
занимают второе место после свинцовых. Токообразующая реакция:
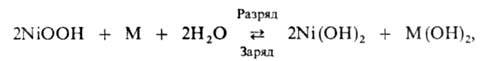
где M-Cd или Fe. Электролит-водный р-р КОН, в к-рый иногда вводят LiOH
для улучшения работоспособности окисноникелевого электрода. НРЦ составляет
1,30-1,34 В для НКА и 1,37-1,41 В для НЖА (спустя нек-рое время после окончания
заряда), уд. энергия 20-35 Вт*ч/кг. Щелочные аккумуляторы имеют, как правило, высокий
ресурс - 1-2 тыс. циклов. Электроды м.б. разл. конструкции: ламельные,
в к-рых активная масса заключена в плоские коробочки-ламели из перфорированной
стальной ленты; спеченные, в к-рых активная масса вводится в поры основы,
образуемой при спекании порошкообразного металлич. Ni; прессованные, в
к-рых активную массу под давл. 35-60 МПа напрессовывают на стальную основу
(толщина пластин 0,8-1,8 мм).
НЖА используют в осн. для изготовления тяговых аккумуляторных батарей
большой емкости (до 1200 А * ч). Они дешевле НКА, но характеризуются повыш.
саморазрядом из-за коррозии железа в щелочном р-ре; кроме того, у них более
низкие значения отдачи по току и по энергии. В НКА не наблюдается коррозии
Cd и связанного с ней газовыделения, что обусловливает большую длительность
сохранения заряженного состояния и возможность полной герметизации аккумулятора. Герметичные
НКА выпускают емкостью от 0,01 до 160 А * ч. Их широко используют как источники
электрич. энергии в приборах бытовой техники, ср-вах связи и т.п.
Серебряно-цинковые аккумуляторы со щелочным электролитом имеют высокую уд. энергию
(до 130 Вт*ч/кг) и способны разряжаться большими токами, но из-за высокой
стоимости серебра нашли применение только в специальных отраслях, напр.
в космической технике. Токообразующая р-ция:
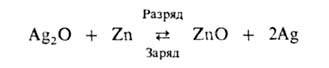
При заряде возможно также образование AgO. Поэтому на зарядных и разрядных
кривых наблюдаются ступени, соответствующие р-циям с участием Ag2O
и AgO. НРЦ 1,60-1,85 В, ресурс не превышает 100-200 циклов.
Попытки замены Ag др. материалами привели к созданию никель-цинковых
аккумуляторах, в к-рых используют спеченный или прессованный окисноникелевый электрод
от НКА и цинковый электрод от серебряно-цинковых аккумуляторов. Токообразующая р-ция:
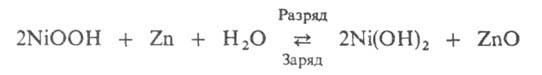
НРЦ 1,74-1,78 В, уд. энергия ок. 60 Вт*ч/кг, ресурс ок. 300 циклов.
Разрабатываемые варианты этих аккумуляторах предназначены в осн. для электромобилей,
но широкому использованию их мешает недостаточный пока ресурс работы.
В никель-водородных аккумуляторах протекает след. токообразующая р-ция:
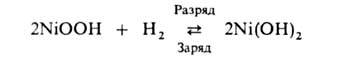
Выделяющийся при заряде Н2 накапливается под давлением. Поэтому
блок с электродами помещают в стальной цилиндр, выдерживающий давления
до 10 МПа. НРЦ 1,32-1,36 В, уд. энергия 50-60 Вт*ч/кг, ресурс неск. тысяч
циклов. Из-за дороговизны произ-ва такие аккумуляторы применяют пока только в космич.
технике.
Среди перспективных конструкций аккумуляторов с неводными электролитами Наиб. интерес
представляют серно-натриевые с твердым керамич. электролитом из алюминатов
натрия, обладающим проводимостью по ионам Na+ . Рабочая т-ра
такого аккумулятора 300-350°С. Токообразующая р-ция:
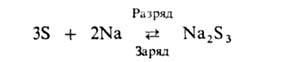
НРЦ 2,08 В. Осн. трудность при разработке: создание технологии изготовления
тонких, но достаточно стойких деталей из твердого электролита. Разрабатывают
также высокотемпературные сульфид-железо-литиевые аккумуляторы; в них вместо твердого
электролита применяют расплав солей, окислителями служат FeS или FeS2.
По своим характеристикам эти аккумуляторы близки к серно-натриевым.
Если требуется более высокое напряжение, чем у отдельного аккумулятора, применяют
аккумуляторные батареи, состоящие из последовательно включенных аккумуляторов, имеющих
общий корпус, выводы и маркировку. Батареи широко применяют в транспортных
ср-вах для запуска двигателей, освещения и др. Тяговые батареи используют
для силовых установок электрокаров, стационарные большой емкости-для электропитания
телефонных сетей, в кач-ве аварийных источников электроэнергии на случай
перебоев в электросети (напр., в операционных). Малогабаритные герметичные
батареи применяют для питания переносных радиоприемников и др. устройств.
Большое внимание уделяется разработке батарей для электромобилей. Мировое
произ-во одних лишь стартерных батарей из свинцовых аккумуляторов превышает 100 млн.
штук в год.
В отличие от гальванич. элементов аккумуляторы требуют ухода при эксплуатации:
их необходимо заряжать, периодически доливать электролит и поддерживать
постоянной его концентрацию, проводить тренировочные и контрольные зарядно-разрядные
циклы и т.п. Разрабатывают т. наз. малообслуживаемые и необслуживаемые
аккумуляторы, уход за которыми упрощен.
===
Исп. литература для статьи «АККУМУЛЯТОРЫ»: Романов В. В., Хашев Ю. М., Химические источники тока,
2 изд., М., 1978; Багоцкий В.С., Скундин А. М., Химические источники тока,
М., 1981. B.C. Багоцкий.
Страница «АККУМУЛЯТОРЫ» подготовлена по материалам химической энциклопедии.
|

