ЭЛЕКТРОЛИТЫ, в-ва, в к-рых в заметной концентрации присутствуют ионы, обусловливающие прохождение электрич. тока (ионную проводимость). Э. также наз. проводниками второго рода. В узком смысле слова Э.-в-ва, молекулы к-рых в р-ре вследствие электролитической диссоциации распадаются на ионы. Различают электролиты твердые, растворы электролитов и ионные расплавы. Р-ры электролитов часто также наз. Э. В зависимости от вида р-рителя различают Э. водные и электролиты неводные. Особый класс составляют высокомол. Э.- полиэлектролиты.
В соответствии с природой ионов, образующихся при электролитич. диссоциации водных р-ров, выделяют солевые Э. (в них отсутствуют ионы Н+ и ОН-), к-ты (преобладают ионы Н+) и основания (преобладают ионы ОН-). Если при диссоциации молекул Э. число катионов совпадает с числом анионов, такие Э. наз. симметричными (1,1 -валентными, напр. КС1, 2,2-валентными, напр. CaSO4, и т.д.). В противном случае Э. наз. несимметричными (1,2-валентные Э., напр. H2SO4, 3,1-валентные, напр. А1(ОН)3, и т.д.).
По способности к электролитич. диссоциации Э. условно разделяют на сильные и слабые. Сильные Э. практически полностью диссоциированы на ионы в разбавленных р-рах. К ним относятся многие неорг. соли, нек-рые к-ты и основания в водных р-рах, а также в р-рителях, обладающих высокой диссоциирующей способностью (напр., в спиртах, амидах, кетонах). Молекулы слабых Э. лишь частично диссоциированы на ионы, к-рые находятся в динамич. равновесии с недиссоциир. молекулами. К слабым Э. относятся многие орг. к-ты и основания в водных и неводных р-рителях. Степень диссоциации зависит от природы р-рителя, концентрации р-ра, т-ры и др. факторов. Один и тот же Э. при одинаковой концентрации, но в разл. р-рителях образует р-ры с разл. степенью диссоциации.
Электролитич. диссоциация приводит к увеличению общего числа частиц в р-ре, что обусловливает существенное различие между св-вами разбавл. р-ров электролитов и неэлектролитов. Этим, в частности, объясняется увеличение осмотич. давления р-ра и его отклонение от закона Вант-Гофа (см. Осмос), понижение давления пара р-рителя над р-ром и его отклонение от Рауля закона, увеличение изменения т-ры кипения и замерзания р-ра относительно чистого р-рителя и др.
Ионы в Э. являются отд. кинетич. единицами и участвуют в хим. р-циях и электрохим. процессах часто независимо от природы др. ионов, присутствующих в р-ре. При прохождении электрич. тока через Э. на погруженных в него электродах происходят окислит.-восстановит. р-ции, в результате чего в своб. виде выделяются в-ва, к-рые становятся компонентами Э. (см. Электролиз).
Э. по своей структуре представляют собой сложные системы, состоящие из ионов, окруженных молекулами р-рителя, недиссоциированных молекул растворенного в-ва, ионных пар и более крупных агрегатов. Св-ва Э. определяются характером ион-ионных и ион-молекулярных взаимод., а также изменением св-в и структуры р-рителя под влиянием растворенных частиц Э. В полярных р-рителях благодаря интенсивному взаимод. ионов с молекулами р-рителя образуются сольватные структуры (см. Сольватация). Роль сольватации с увеличением валентности ионов и уменьшением их кристаллографич. размеров возрастает. Мерой взаимод. ионов с молекулами р-рителя является энергия сольватации.
В зависимости от концентрации Э. выделяют область разбавленных р-ров, к-рые по своей структуре близки к структуре чистого р-рителя, нарушаемой, однако, присутствием и влиянием ионов; переходную область и область концентрир. р-ров. Весьма разбавленные р-ры слабых Э. по своим св-вам близки к идеальным р-рам и достаточно хорошо описываются классич. теорией электролитич. диссоциации. Разбавленные р-ры сильных Э. заметно отклоняются от св-в идеальных р-ров, что обусловлено электростатич. межионным взаимод. Их описание проводится в рамках Дебая-Хюккеля теории, к-рая удовлетворительно объясняет концентрационную зависимость термодинамич. св-в - коэф. активности ионов, осмотич. коэф. и др., а также неравновесных св-в -электропроводности, диффузии, вязкости (см. Электропроводность электролитов). При повышении концентрации р-ров сильных Э. возникает необходимость в учете размера ионов, а также влияния сольватационных эффектов на характер межионного взаимодействия.
В переходной концентрационной области под влиянием ионов происходит существенное изменение структуры р-рителя. При дальнейшем увеличении концентрации Э. почти все молекулы р-рителя связаны с ионами в сольватационные структуры и обнаруживается дефицит р-рителя, а в области концентрированных р-ров структура р-ра все более приближается к структуре соответствующих ионных расплавов или кристаллосольватов. Данные компьютерного моделирования и спектроскопич. исследований, в частности методом рассеяния нейтронов с изотопным замещением, свидетельствуют о значит. степени упорядоченности в концентрированных р-рах Э. и об образовании специфич. для каждой конкретной системы ионных структур. Напр., для водного р-ра NiCl2 характерен комплекс, содержащий ион Ni2+, окруженный 4 молекулами воды и 2 ионами Сl- в октаэдрич. конфигурации. Ионные комплексы связываются между собой посредством связей галоген - водород - кислород и более сложных взаимод., включающих молекулы воды.
В ионных расплавах специфика упорядочения характеризуется структурными факторами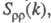 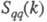 и и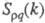 , описывающими флуктуации ионной плотности , описывающими флуктуации ионной плотности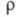 и заряда q как ф-ции волнового числа k, к-рое с точностью до постоянной Планка h совпадает с величиной импульса, передоваемого расплаву рассеивающей частицей, напр. нейтроном. Для бинарного электролита и заряда q как ф-ции волнового числа k, к-рое с точностью до постоянной Планка h совпадает с величиной импульса, передоваемого расплаву рассеивающей частицей, напр. нейтроном. Для бинарного электролита
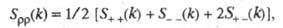
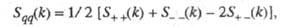
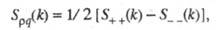
где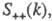 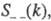 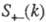 - парциальные структурные факторы, относящиеся к взаимод. катионов и анионов между собой и друг с другом. Для расплавов типа NaCl ф-ция - парциальные структурные факторы, относящиеся к взаимод. катионов и анионов между собой и друг с другом. Для расплавов типа NaCl ф-ция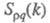 близка к нулю, вследствие чего Э. можно рассматривать как смесь двух жидкостей, одна из к-рых характеризуется упорядочением по ионной плотности через ф-цию близка к нулю, вследствие чего Э. можно рассматривать как смесь двух жидкостей, одна из к-рых характеризуется упорядочением по ионной плотности через ф-цию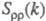 , а вторая -"зарядовым" упорядочением через ф-цию , а вторая -"зарядовым" упорядочением через ф-цию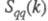 . Ф-ция . Ф-ция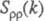 имеет типичное поведение для систем с "плотностным" упорядочением, отражая значит. степень беспорядка в расположении частиц. В отличие от этого имеет типичное поведение для систем с "плотностным" упорядочением, отражая значит. степень беспорядка в расположении частиц. В отличие от этого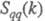 имеет резкий пик, отражающий сильное упорядочение в распределении заряда, определяемое экранированием и требованиями локальной электронейтральности. Такое упорядочение ионов приводит к возможности существования в Э. коллективных возбуждений, к-рые могут проявляться в виде пиков динамич. структурного фактора имеет резкий пик, отражающий сильное упорядочение в распределении заряда, определяемое экранированием и требованиями локальной электронейтральности. Такое упорядочение ионов приводит к возможности существования в Э. коллективных возбуждений, к-рые могут проявляться в виде пиков динамич. структурного фактора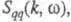 описывающего динамику флуктуации плотности заряда расплава ( описывающего динамику флуктуации плотности заряда расплава (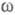 - частота, связанная с энергией, передаваемой расплаву рассеивающей частицей). Для ионных расплавов Э., катионы к-рых склонны к образованию ковалентных связей с анионами (напр., для расплава CuCl), наблюдается сильная корреляция взаимод. между анионами и довольно слабая - между катионами. - частота, связанная с энергией, передаваемой расплаву рассеивающей частицей). Для ионных расплавов Э., катионы к-рых склонны к образованию ковалентных связей с анионами (напр., для расплава CuCl), наблюдается сильная корреляция взаимод. между анионами и довольно слабая - между катионами.
Переход от одной концентрационной области Э. в другую происходит плавно, вследствие чего рассмотренное выше деление является условным. Тем не менее в промежут. области нек-рые термодинамич. св-ва Э., напр. коэф. р-римости, претерпевают заметные изменения. Описание промежут. и концентрационной областей требует явного рассмотрения как ионов, так и молекул р-рителя и учета разл. видов взаимод. между всеми частицами в р-ре.
В зависимости от т-ры и давления выделяют низкотемепературную и высокотемпературную области св-в Э., а также области нормальных и высоких давлений. Повышение т-ры или давления в целом снижают мол. упорядоченность р-рителя и ослабляет влияние ассоциативных и сольватационных эффектов на св-ва р-ра Э. При понижении т-ры иже т-ры плавления нек-рые концентрир. Э. могут находиться стеклообразном состоянии, напр. водные р-ры LiCl.
Наряду с Э. как проводниками второго рода существуют в-ва, обладающие одновременно электронной и ионной проводимостью. К ним относятся р-ры щелочных и щел.-зем. металлов в полярных р-рителях (аммиак, амины, эфиры), а также в расплавах солей. В этих системах при изменении концентрации металла происходит фазовый переход в металлич. состояние с существенным (на неск. порядков) изменением электропроводности. При этом в электролитич. области образуется самый легкий анион-сольватированный электрон, придающий р-ру характерный синий цвет.
Э. играют важную роль в науке и технике. Они участвуют в электрохим. и многих биол. процессах, являются средой для орг. и неорг. синтеза и электрохим. произ-в. Изучение св-в Э. важно для выяснения механизмов электролиза, электрокатализа, электрокристаллизации, коррозии металлов и др., для совершенствования механизмов разделения в-в - экстракции и ионного обмена. Исследование св-в Э. стимулируется энергетич. проблемами (создание новых топливных элементов, солнечных батарей, электрохимических преобразователей информации), а также проблемами защиты окружающей среды.
Лит.: Харнед Г., Оуэн Б., Физическая химия растворов электролитов, пер. с англ., М., 1952; Термодинамика и строение растворов. Материалы симпозиума "Химия водных систем при высоких температурах и давлениях", Иваново, 1986; March N.H., Тоsi M. P., Coulomb liquids, L.-[a.o.], 1984; см. также лит. к ст. Растворы электролитов, Электропроводность электролитов, Электролиты неводные, Электролиты твердые.
М. Ф. Головко.
|

