|
ХИМИЧЕСКОЕ РАВНОВЕСИЕ, термодинамич.
равновесие в системе, между компонентами к-рой происходят хим. р-ции. Для
данной р-ции где Аi - исходные реагенты; Вj - продукты;
vi и vj - их стехиометрич. коэффициенты
соотв., X. р. достигается при условии:
где Аi - исходные реагенты; Вj - продукты;
vi и vj - их стехиометрич. коэффициенты
соотв., X. р. достигается при условии:
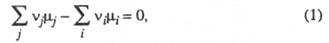
где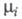 и и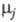 -
хим. потенциалы соотв. исходных реагентов и продуктов. -
хим. потенциалы соотв. исходных реагентов и продуктов.
Условие X. р. может быть выведено из любого
условия термодинамического равновесия, в частности из условия минимума
энергии Гиббса системы dGT,p = 0 при постоянных абс.
т-ре Т и давлении р.
К условию X. р. (1) добавляется требование
постоянства т-ры и давления по всему объему системы (в случае гетерогенных
р-ций для X. р. необходимо, чтобы т-ра и давление были одинаковы во всех
фазах системы).
В состоянии X. р. система характеризуется
константой равновесия Ка , выражающей для р-ций в р-рах
соотношение между активностями аАi исходных реагентов
и активностями аBj продуктов:

(П - знак произведения). В случае идеальных
р-ров вместо активностей компонентов используют их молярные доли xi.
Для р-ций в газах активности в-в заменяют летучестями (константа равновесия
Kf); если реагирующую систему можно считать идеальной
газовой смесью, вместо летучестей возможно применение парциальных давлений
компонентов (константа равновесия Кр). Для идеальных
систем соотношение (2) наз. действующих масс законом.
Помимо термодинамич. определения X. р.,
к-рое выражается соотношением (1), существует и кинетич. определение: X.
р. устанавливается при условиях, когда скорость прямой р-ции (исходные
реагенты продукты)
v становится равной скорости обратного превращения (продукты продукты)
v становится равной скорости обратного превращения (продукты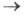 исходные реагенты) v-1. Константа равновесия
исходные реагенты) v-1. Константа равновесия

где k1 и k-1
- константы скорости прямой и обратной р-ций соотв. Кинетич. определение
подчеркивает динамич. характер X. р.: при его достижении р-ции в системе
не прекращаются. Если в системе происходят несколько связанных между собой
хим. р-ций, кинетич. определение X. р. (3) выполняется, когда справедлив
детального равновесия принцип, т. е. для каждой из р-ций достигается
равенство скоростей в прямом и обратном направлениях. Напр., если в системе
протекает циклич. превращение
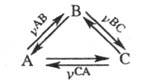
и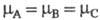 (термодинамич. условие X. р.), то обязательно
(термодинамич. условие X. р.), то обязательно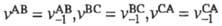 (кинетич. определение).
(кинетич. определение).
Отклонение от Х. р. сопровождается изменением
состава системы и м. б. выражено химическим сродством р-ции А.
Устойчивость X. р. определяется условием:
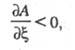
где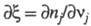 - степень полноты р-ции, равная отношению изменения числа молей nj,
любого из участвующих в р-ции в-в к его стехиометрич. коэф. vj.
- степень полноты р-ции, равная отношению изменения числа молей nj,
любого из участвующих в р-ции в-в к его стехиометрич. коэф. vj.
Для нек-рых неравновесных систем м. б.
использовано понятие локального Х. р., к-рое устанавливается в малом объеме
системы и соответствует локальным значениям т-ры, давления, хим. потенциалов
компонентов.
Важной практич. задачей является термодинамич.
расчет X. р., т. е. определение равновесных составов системы. В совр. компьютерных
программах такой расчет, как правило, выполняется путем прямой минимизации
энергии Гиббса системы без использования констант равновесия. Для идеальных
систем результатом расчетов являются концентрации хим. в-в в состоянии
равновесия, для реальных систем мат. определение концентрации требует дополнительно
знания коэф. активности (или летучести).
Лит. см. при ст. Химическая термодинамика.
М. В. Коробов.
===
Исп. литература для статьи «ХИМИЧЕСКОЕ РАВНОВЕСИЕ»: нет данных
Страница «ХИМИЧЕСКОЕ РАВНОВЕСИЕ» подготовлена по материалам химической энциклопедии.
|

